Les travaux de Christopher Fernandez Prada, professeur agrégé au Département de pathologie et microbiologie à la Faculté de médecine vétérinaire de l’Université de Montréal, et ses collègues, Martin Olivier, professeur au département de microbiologie et d’immunologie de l’Université McGill, David Langlais, professeur au département de génétique humaine au Centre de génomique de l’Université McGill, ont permis de réaliser une découverte fondamentale qui révolutionne la recherche sur la propagation de la résistance aux antimicrobiens et le traitement de la leishmaniose.
Sur la photo de gauche à droite : David Langlais, cochercheur de l'étude; Atia Amin, doctorante; Noélie Douanne, doctorante et première auteure de l'étude; George Dong, doctorant; Martin Olivier, cochercheur de l'étude; Christopher Fernandez-Prada, cochercheur de l'étude. Photo : Aida Minguez-Menéndez. |
La résistance aux antimicrobiens constitue depuis longtemps un enjeu de santé publique. Nous savons que les bactéries « communiquent » entre elles pour échanger leurs gènes, un phénomène à l’origine de la résistance aux antibiotiques. La résistance aux médicaments est aussi observée chez les cellules eucaryotes, mais leur mécanisme de transmission était jusqu’à maintenant inconnu. Les eucaryotes sont composés d'organismes pluricellulaires, comme les animaux et les plantes et d’unicellulaires, comme le parasite Leishmania, sur lequel l’équipe de recherche s’est concentrée.
Les eucaryotes libèrent des vésicules extracellulaires, soit de minuscules particules rondes. Ces vésicules ont été découvertes il y a une vingtaine d’années, mais personne ne savait ce qu’elles contenaient, ni comment elles interagissaient. L’équipe de chercheurs s’est donc demandée si ces vésicules pouvaient jouer un rôle dans la transmission de la résistance aux médicaments. « Nous suspections qu'il y avait un échange autre que la division cellulaire, mais cela n’avait jamais été observé jusqu’à maintenant », explique M. Fernandez Prada. Ils ont en effet découvert que le transfert de gènes était possible entre cellules eucaryotes. Elles transmettent leur ADN par le biais de ces vésicules extracellulaires. Cette découverte est déterminante en biotechnologie. « Les vésicules modulent le système immunitaire, contrôlent la communication intercellulaire et sont responsables du transfert des gènes de résistance », résume-t-il.
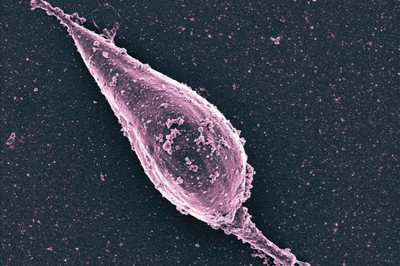
Parasite Leishmania avec vésicules extracellulaires. |
La découverte de Christopher Fernandez Prada et son équipe ouvre la porte à de nouvelles pistes de solutions pour le traitement de la leishmaniose. « Nous tentons de voir s’il est possible d’inhiber ou d’empêcher le transfert de vésicules par les parasites ». En « bloquant » le mode de communication entre parasites, la propagation de la résistance est limitée.
L’équipe estime que cette découverte pourrait s’appliquer à n’importe quel type d’eucaryote. Des travaux de recherche sont en cours pour le démontrer. « Nous testons différentes cellules pour observer leur contenu ». Une cellule eucaryote comme Leishmania fait tout juste 15 microns. L’ADN contenu dans une cellule est infime. Une vésicule mesure entre 150 et 250 nanomètres, ce qui est incroyablement petit. « Nous avons maintenant accès à des appareils technologiques puissants qui nous permettent de récupérer l’ADN contenu dans une vésicule afin de le séquencer et l’observer en détail ».
Les cellules cancéreuses relâchent aussi des vésicules extracellulaires. La découverte de M. Fernandez Prada et son équipe vient ainsi alimenter la recherche contre le cancer. « Nous tentons de déterminer si la résistance aux antitumoraux peut être remédiée avec les vésicules extracellulaires. Cette hypothèse suscite énormément d’intérêt », explique-t-il.
La leishmaniose : une maladie infectieuse planétaire
Leishmania, l’eucaryote analysé par M. Fernandez Prada et son équipe, peut parasiter les animaux et les humains. Il est responsable de causer la leishmaniose, une infection tropicale négligée qui touche près de 15 millions de personnes sur le globe1. Entre 700 000 et 1 million de nouveaux cas sont déclarés par année2, et il n’existe actuellement aucun vaccin préventif au traitement définitif. Ce parasite peut occasionner la formation d’ulcères cutanés et s’attaquer aux organes internes, comme la rate et le foie, en détruisant les cellules. Une fois contractée, la leishmaniose est une maladie à vie. La forme viscérale de la maladie peut également s’avérer mortelle si non traitée.
Il est assez ironique de penser que l’élément déclencheur d’une maladie qui touche des millions de sujets sur la planète est en fait… un phlébotome, une minuscule mouche de sable. Les phlébotomes femelles jouent le rôle de vecteurs de la maladie en se nourrissant du sang d’animaux infectés. En prenant leur « prochain repas » sur un humain, les mouches infectées crachent du mucus contenant les parasites dans la peau de leur hôte. C’est ainsi que s’enclenche le cycle d’infection, à partir d’une interaction entre insectes, animaux et humains.
Les chiens sont considérés comme réservoirs de la maladie, bien que la leishmaniose touche plusieurs mammifères. « Les chiens ont été identifiés comme réservoirs, simplement parce que c'est l'animal de compagnie qui se retrouve le plus fréquemment en contact avec l’humain », explique M. Fernandez Prada. Si les phlébotomes sont à proximité, la transmission du parasite est facilitée.

Le réchauffement climatique, ainsi que les mouvements de population ont contribué à la propagation des cas au cours des dernières années. La leishmaniose se retrouve désormais dans les régions subtropicales, dont le sud des États-Unis. « Il n’y a toutefois pas de problème de leishmaniose au Canada », précise M. Fernandez Prada.
Efficacité restreinte des traitements disponibles
Les médicaments disponibles à l’heure actuelle ne guérissent pas complètement les patients. La même molécule est utilisée depuis une centaine d'années. Il s’agit d’un dérivé de l'antimoine, qui est un métal. L’antimoine est très agressif et toxique, autant pour les parasites que l’humain et l’animal, et génère de nombreux effets secondaires. Comme ce composé chimique a été utilisé durant de nombreuses années, l’apparition de résistance sévère a été observée, notamment dans les pays endémiques, comme l’Inde.
Vers les années 2000, la leishmaniose est devenue très préoccupante en Inde, où est répertoriée une forme viscérale de la maladie, appelée kala-azar (ou fièvre noire). La miltéfosine a alors été introduite pour traiter les patients. Toutefois, comme cette molécule sélectionne rapidement la résistance, les recherches ont bifurqué vers l'amphotéricine B, un antifongique. L'amphotéricine B est utilisé en dernier recours chez les humains, pour préserver son efficacité thérapeutique et éviter qu’il ne se développe de la résistance. « C’est la seule molécule qui ne peut pas être employée pour traiter les chiens », précise M. Fernandez Prada.
Une stratégie Une seule santé pour la gestion de la leishmaniose
Une approche intégrée doit être privilégiée dans la lutte contre cette maladie complexe qui touche à la fois les animaux et les humains, et qui prend de l’ampleur avec les changements climatiques. La gestion de la leishmaniose s’inscrit dans une perspective Une seule santé, puisque la santé humaine, la santé animale et celle des écosystèmes sont interconnectées. Elle nécessite une collaboration des acteurs en médecine humaine et en médecine vétérinaire, ainsi que des experts en environnement, de concert avec les autorités compétentes.
M. Fernandez Prada donne un bon exemple de l’interdépendance des éléments, en renvoyant à une intervention ratée datant de la Deuxième Guerre mondiale. À l’époque, des milliers de soldats étaient infectés par la malaria (paludisme). Des pesticides ont été utilisés de façon massive en Italie pour éliminer les moustiques responsables de la transmission de la maladie. Or, ces moustiques sont devenus eux-mêmes résistants aux pesticides. « Ce sont des interventions dangereuses d’un point de vue écologique. Elles tuent des insectes en masse, créant un déséquilibre des écosystèmes ». D’où l’importance d’appliquer des mesures concertées.
La leishmaniose se trouve dans la liste des maladies tropicales négligées recensées par l’Organisation mondiale de la santé (OMS). L’industrie pharmaceutique a manifesté peu d’intérêt pour développer des traitements, comme c’est le cas pour nombre de maladies tropicales répertoriées dans les pays en voie de développement. La situation est néanmoins en train d’évoluer.
Des solutions à l’horizon
Il est possible de ralentir la transmission de Leishmania par la mouche de sable en agissant sur le développement de la résistance. C’est d’ailleurs ce que vise à accomplir M. Fernandez Prada, en « neutralisant » les vésicules extracellulaires des cellules eucaryotes.
 | « Les médecins vétérinaires et les chercheurs en médecine vétérinaire peuvent concrètement contribuer à l’aspect Une seule santé dans le traitement de la leishmaniose. » - Christopher Fernandez Prada |
En plus de ses travaux sur les eucaryotes, Christopher Fernandez Prada s’affaire au développement d’un nouveau traitement contre la leishmaniose, appuyé par William Lubel, chimiste à l’Université de Montréal. « Nous sommes en processus de dépôt de demande de brevet et nous avons obtenu du financement en vue de produire de nouvelles molécules contre les parasites protozoaires. Parmi ces parasites, nous avons ciblé Leishmania, responsable de la leishmaniose, et le trypanosome, qui cause la maladie de Chagas3 (trypanosomiase américaine) et la maladie du sommeil4 (trypanosomiase africaine) ». Ces maladies sont transmises par des vecteurs et appartiennent à la même famille. « William Lubel a développé des molécules que nous avons testées dans différents modèles de parasites ». L’équipe a réalisé le criblage des molécules dans des parasites déjà résistants à d’autres molécules, une procédure innovatrice. Ils ont obtenu des molécules capables de détruire les parasites résistants aux médicaments en circulation. Les tests réalisés sur des modèles animaux ont démontré des résultats très prometteurs.
Ces travaux de recherche sont aussi menés en collaboration avec Martin Olivier, de l’Université McGill, ainsi qu’Ada E. Yonath, professeure au Département de biologie chimique et structurale du Weizmann Institute of Science en Israël. Mme Yonath a obtenu le prix Nobel de chimie en 2009 pour ses découvertes sur la structure des ribosomes, qui sont des synthétiseurs des protéines de nos cellules. « Nous croyons que des molécules attaquent les ribosomes des parasites », explique M. Fernandez Prada.
Comme pour tout développement de solution thérapeutique, il s’agit d’un long processus. « Nous sommes à l’étape de l’étude de marché afin d’approcher différents joueurs ». Des essais cliniques en médecine humaine devront être réalisés, avec le soutien d’un partenaire pharmaceutique.
Mesures préventives et éducation
Différentes mesures préventives doivent être mises en place pour contenir la propagation de leishmaniose. Une mesure toute simple peut être, par exemple, d’installer des moustiquaires aux portes et fenêtres afin d’éviter les piqûres d’insectes. En médecine vétérinaire, la prévention est bien ancrée dans la pratique de façon générale. Les patients sont souvent traités en amont pour éviter l’apparition de problèmes de santé. « Dans le cas de la leishmaniose, l’adoption d’une approche préventive en médecine vétérinaire permettrait de réduire considérablement les bassins de résistance, et aurait un impact positif, autant chez l’animal que l’humain ». Il existe un vaccin pour traiter la leishmaniose canine, mais pour être pleinement efficace, l’animal a besoin d’une dose de rappel par année. Ce vaccin est en outre très onéreux.
Un volume considérable d’animaux peut traverser les frontières canadiennes chaque année, que ce soit dans un contexte de voyage, d’immigration, ou encore, d’importation d’animaux de l’étranger. Afin d’éviter l’introduction de maladies au pays, l’Agence canadienne d’inspection des aliments (ACIA) a instauré des règles pour encadrer le transport et l’importation d’espèces animales via nos frontières.
Les chiens doivent être vaccinés contre la rage pour entrer au Canada. Il n’y a présentement aucune précaution exigée contre la leishmaniose, puisque le Canada n’est pas un pays endémique. Pourtant, au cours des trois dernières années, une quarantaine de chiens infectés par le parasite Leishmania sont arrivés à Montréal par voie aérienne. Un chien peut être infecté sans présenter de signes cliniques. Or, de longues heures de transport peuvent affaiblir le système immunitaire de l’animal et déclencher des signes cliniques.
« Nous travaillons à éduquer encore plus les membres de la communauté vétérinaire sur la leishmaniose ». Les futurs médecins vétérinaires reçoivent de la formation sur les maladies tropicales afin de les préparer à identifier et à traiter ces cas. Des démarches sont également en cours afin de réclamer de nouveaux protocoles et un accès plus étendu aux traitements et aux méthodes de prévention, dont les vaccins canins. Certaines solutions pourraient être mises à la disposition des propriétaires d’animaux pour prévenir les piqûres de phlébotomes. Par exemple, en Amérique du Sud et en Europe, les chiens peuvent porter des colliers antimoustiques qui contiennent un insecticide (pyréthrine).
« Nous collaborons aussi davantage avec nos collègues en santé publique afin que les infectiologues et les omnipraticiens au Québec soient mieux formés en maladies infectieuses tropicales ».
_____________________
1 Source : Noélie Douanne, George Dong, Atia Amin, Lorena Bernardo, Mathieu Blanchette, David Langlais, Martin Olivier, Christopher Fernandez-Prada,Leishmania parasites exchange drug-resistance genes through extracellular vesicles, Cell Reports, Volume 40, Issue 3, 2022, 111121, ISSN 2211-1247, doi.org/10.1016/j.celrep.2022.111121.
2 Source : Leishmaniose, Organisation mondiale de la Santé.
3 La maladie de Chagas, aussi connue sous le nom de trypanosomiase américaine, est une maladie potentiellement mortelle provoquée par le protozoaire Trypanosoma cruzi. (Source: Organisation mondiale de la Santé).
4 La trypanosomiase africaine, connue aussi sous le nom de maladie du sommeil, est une maladie transmise par une mouche tsé-tsé infectée, que l'on trouve dans certaines régions rurales de l'Afrique subsaharienne. La maladie du sommeil est causée par deux différents parasites, le Trypanosoma brucei rhodesiense et le Trypanosoma brucei gambiense. La plupart des cas signalés de maladie du sommeil sont causés par le Trypanosoma brucei gambiense. (Source : Gouvernement du Canada).